光療技術如光動力療法療法(PDT)和光熱療法(PTT)因其具有微創性的優點等在癌癥治療技術引起了廣泛關注。然而,傳統的 PDT/PTT 試劑通常存在著成像效率低和無成像能力的缺點。近年來,金屬納米粒子偶聯物被證明具有一種新型的聚集誘導發射,使其成為具有吸引力的多功能治療劑。在這里,該研究設計了單光子和雙光子激發熒光,單線態氧(1O2)產生和光熱效應的Ce6共軛金納米顆粒(AuNPs)。Ce6-Au NPs的光活性在單獨形式下受到抑制,在聚集形式下顯著增強,并且由于發射壽命縮短而顯著改善了光穩定性。通過在癌細胞內形成聚集體,利用聚集的 Ce6-Au NPs分別在紅外和近紅外光的單光子和雙光子激發下作為熒光成像探針。聚集的 Ce6-Au NPs還表現出優異的PDT 和PTT 性能,并且能夠通過使用功率密度低于皮膚耐受閾值的紅光連續波激光有效地根除癌細胞。這種等離子體納米系統為成像引導的 PDT/PTT 協同治療提供了一個有前途的潛力,可能為探索安全、無創的治療開辟一個新的場所。
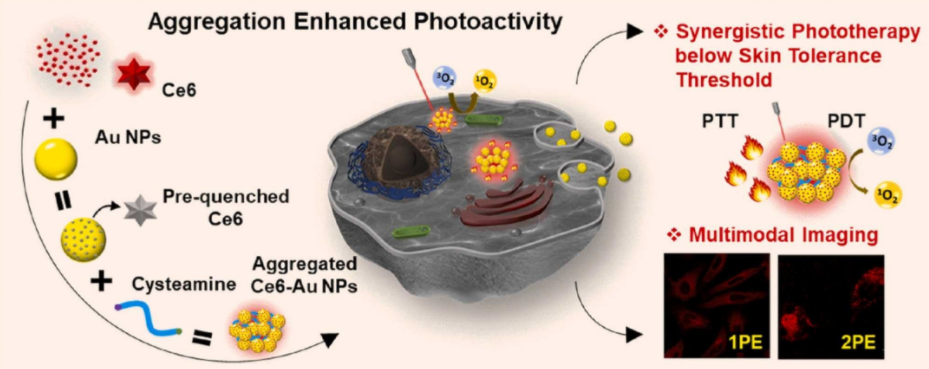
圖1. 聚集誘導等離子體增強熒光及抗腫瘤研究
Ce6分子可以通過配位作用緊密吸附在金納米粒子的表面上。聚集態Ce6-Au NPs的 LSPR 譜帶與 Ce6的吸收光譜和熒光光譜有重疊。當與Ce6結合時,Au NPs的LSPR 帶略有紅移。通過 DTT 置換將吸附的 Ce6分子從Au NP分離并根據 Au NP 和分離的 Ce6分子的消光度計算它們的摩爾比來確定在 Au NP 表面上吸附的Ce6分子的量。吸附在金納米粒子表面的 Ce6的相應熒光猝滅了約89%。
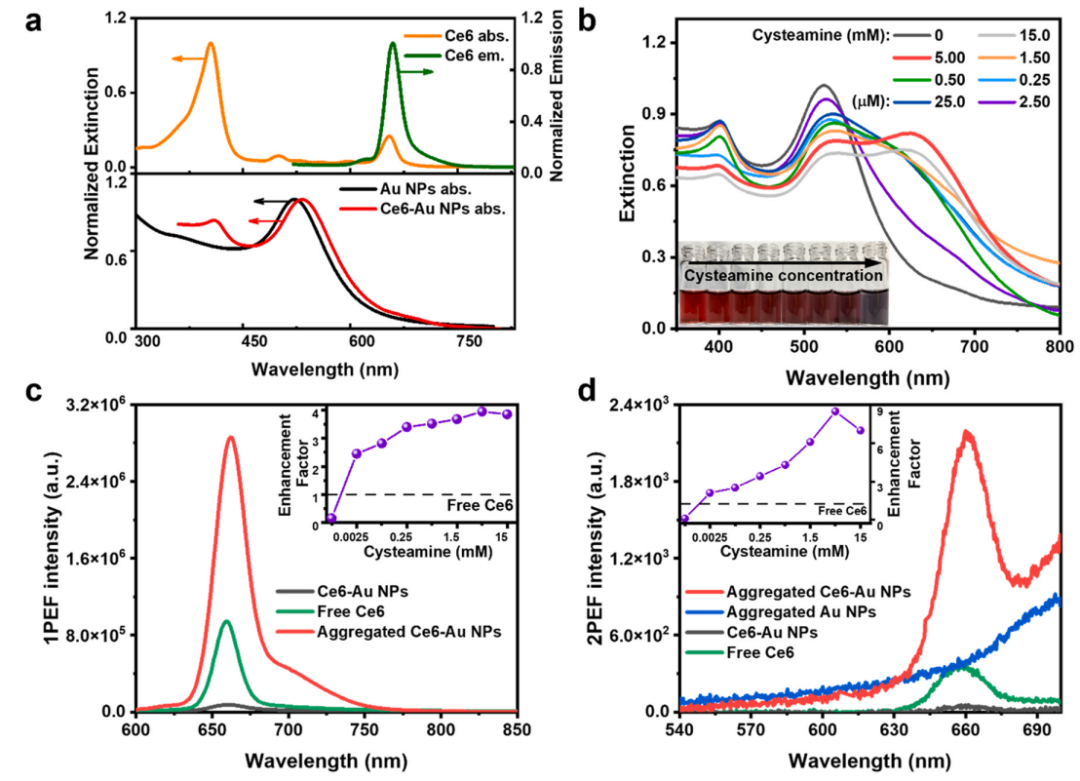
圖2. 材料表征
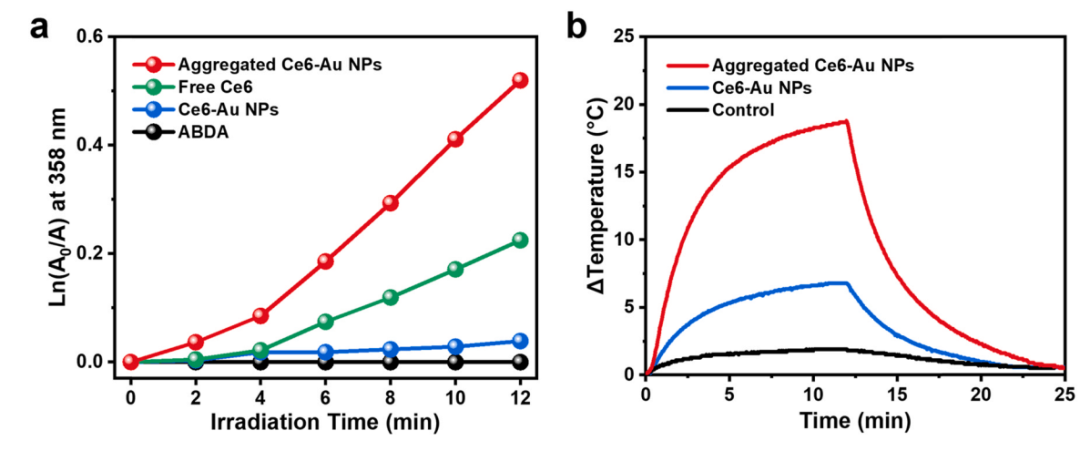
圖3. (a)在游離的 Ce6,分離的和聚集的 Ce6-Au NPs 存在下,ABDA 的光氧化作為輻照時間的函數。(b) Ce6-Au 納米粒子在連續激光照射下12分鐘后關閉的水分散體的光熱效應。
用游離 Ce6處理的癌細胞的共聚焦激光掃描顯微鏡圖像的結果,在633nm激發下分離和聚集的 Ce6-Au NPs。在與Ce6-Au NPs孵育之前,通過與半胱胺預孵育在癌細胞內原位形成聚集的Ce6-Au NPs。用聚集的 Ce6-Au NPs 處理的細胞的熒光圖像顯示最好的對比度,比用游離Ce6處理的細胞的紅色發射強得多,而用分離的 Ce6-Au NPs 處理的細胞的熒光圖像顯示最差的對比度。它們的熒光圖像的相對亮度與它們在溶液中的相對熒光強度一致。在用半胱胺和 Ce6-Au NPs 處理的癌細胞的細胞質中觀察到強烈的紅色發射,表明這些納米顆粒的有效細胞攝取和來自聚集的 Ce6-Au NPs 的熒光起源。這些結果也證實,盡管在溶液和細胞中的環境不同,Ce6-Au NPs確實在原位形成聚集體,并且在這些 HeLa 細胞中保持聚集體的形式。
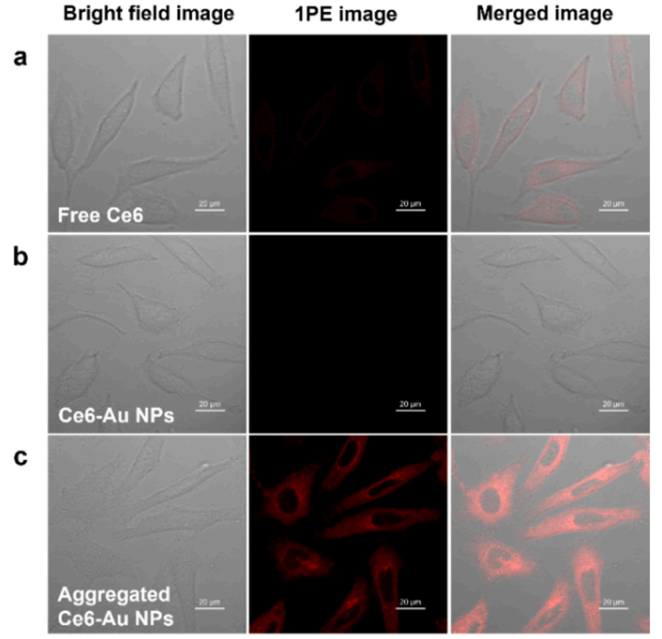
圖4. 與游離 Ce6,分離和聚集的 Ce6-Au NPs 溫育的 HeLa 癌細胞的明場圖像(左) ,1PE 熒光圖像(中)和合并圖像(右)。