由于現有的測試材料在質子治療劑量測定中產生很大的不確定性,導致“射程”的相對差異高達8%。因此,這些現有材料不能為質子治療劑量測定提供準確的質量保證。
相比之下,NPL開發的新材料在1%~2%的精度內模仿質子治療中的人體組織特性,可更加有效地測量復雜質子治療計劃和臨床試驗中的劑量。這種新型組織模擬材料已被用來開發模擬頭頸部腫瘤患者放射治療的裝置。這項研究已發表在Physics in Medicine Biology上。

這是第一個制定組織等效材料的模型,不僅考慮光子相互作用,還考慮質子阻止本領、核吸收和散射相互作用。研究還將優化材料的組織等效性與現有商業組織等效材料進行比較,以評估性能以及改進方面,見圖1。
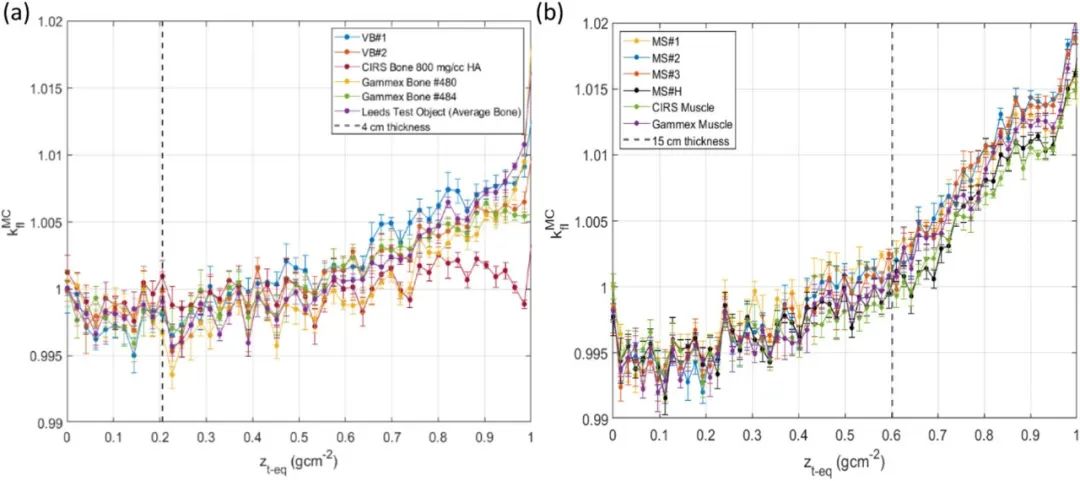
圖1.新配方和商業材料的通量校正因子;(a)椎骨組織等效材料;(b)肌肉組織等效材料;參考虛線突出顯示了質子可能穿過的患者體內每個靶區組織的最大組織厚度(骨骼為4厘米,肌肉為15厘米);每個誤差條都呈現A類不確定性
這些材料使質子中心能夠在臨床使用前檢查和測試質子治療的具體治療情況,使用內部探測器直接測量劑量,并將其與治療計劃軟件的預測值進行比較。這些測試可提高質子中心進行質子治療的準確度。
NPL科學家Ana Lourenço表示:“我們正在與醫學物理與工程研究所(IPEM)合作,制定質子參考劑量測定的新實踐規范(CoP)。即將推出的IPEM CoP將利用NPL的PSPC為質子治療提供劑量校準服務。”
這一進展將減少劑量輸送的不確定性,確保最佳的腫瘤控制,并提高質子治療的準確性。CoP一致標準的建立不僅將使治療機構內和治療機構之間的患者獲益,而且為質子治療臨床試驗的發展奠定基礎。
NPL科學領域負責人Russell Thomas表示:“我們團隊多年來一直致力于測定質子束流的劑量,還開發了用于質子放射治療的專用標準。在此基礎上,我們能夠進一步完善臨床電離室反應的理解。此外,我們還制定了臨床審查方案,確保患者得到最佳治療,并且專門開發了自己的材料來模擬質子束流中組織、骨骼等的反應。”