腫瘤治療后進(jìn)行療效評(píng)價(jià)是臨床醫(yī)師制定患者后續(xù)治療方案或研究者進(jìn)行研究設(shè)計(jì)的重要依據(jù)。雖然循證醫(yī)學(xué)強(qiáng)調(diào)終點(diǎn)(endpoint)指標(biāo)的重要性,但替代終點(diǎn)(surrogate ednpoint)指標(biāo)仍是臨床或研究中作出決策最常用的依據(jù)。通過(guò)終點(diǎn)/替代終點(diǎn)指標(biāo)的檢測(cè)并予以臨床驗(yàn)證,逐步形成了目前我們大量使用的各種“標(biāo)準(zhǔn)”。這些標(biāo)準(zhǔn)的使用促進(jìn)了臨床試驗(yàn)的發(fā)展,加強(qiáng)了學(xué)術(shù)交流。同時(shí),這些標(biāo)準(zhǔn)本身也與時(shí)俱進(jìn),隨著自身和其他學(xué)科的發(fā)展不斷修訂,以適應(yīng)和促進(jìn)臨床醫(yī)學(xué)的發(fā)展。
實(shí)體瘤療效評(píng)價(jià)標(biāo)準(zhǔn)的發(fā)展歷史
實(shí)體瘤療效評(píng)價(jià)標(biāo)準(zhǔn)的發(fā)展已有近40年的歷史。早在1979年,世界衛(wèi)生組織WHO定義了腫瘤療效評(píng)估的方法,該標(biāo)準(zhǔn)定義了實(shí)體瘤雙徑測(cè)量的療效評(píng)價(jià)標(biāo)準(zhǔn),即測(cè)量所有腫瘤的最大平面范圍并將所有值相加,比較兩次檢查間的所有腫瘤平面最大值之和。
1985年,相關(guān)研究發(fā)現(xiàn)臨床試驗(yàn)療效評(píng)價(jià)的偏倚有5%-10%是因?yàn)閃HO標(biāo)準(zhǔn)對(duì)有些病灶的定義模糊和腫瘤測(cè)量上的誤差造成的。這顯然會(huì)降低評(píng)估結(jié)果的可比性,并且影響結(jié)論的可靠性。
1999年研究者們提出了以腫瘤最長(zhǎng)徑的長(zhǎng)度代替面積來(lái)代表腫瘤大小的一維測(cè)量方法(或稱單徑測(cè)量法),并于2000年,發(fā)布了RECIST 1.0標(biāo)準(zhǔn),2009年RECIST標(biāo)準(zhǔn)更新為1.1版本。
這些標(biāo)準(zhǔn)雖然在WHO標(biāo)準(zhǔn)的基礎(chǔ)上簡(jiǎn)化了測(cè)量步驟,提升了準(zhǔn)確性,但仍然是根據(jù)傳統(tǒng)影像(CT、MR)測(cè)量腫瘤大小的變化來(lái)判斷療效。實(shí)際上,許多腫瘤治療后在體積上的變化并不明顯,例如淋巴瘤、肉瘤、肝癌等。因此用RECIST標(biāo)準(zhǔn)并不能很好的反映真實(shí)的療效。
2009年,Prof. Wahl等人首次在JNM上發(fā)表PERCIST (Positron Emission tomography Response Criteria In Solid Tumor) 腫瘤療效評(píng)估標(biāo)準(zhǔn)。PERCIST標(biāo)準(zhǔn)在評(píng)估過(guò)程中引入了功能學(xué)影像信息,即PET/CT的FDG代謝影像信息。根據(jù)腫瘤的代謝程度,對(duì)比前后腫瘤的代謝趨勢(shì)進(jìn)行療效評(píng)估,而非單純的對(duì)比腫瘤的大小。大量臨床研究顯示,與其他標(biāo)準(zhǔn)(WHO, RECIST)相比,PERCIST標(biāo)準(zhǔn)評(píng)估腫瘤療效的準(zhǔn)確性更高。
PERCIST實(shí)體瘤療效評(píng)估標(biāo)準(zhǔn)
PERCIST標(biāo)準(zhǔn)中將腫瘤療效分為四個(gè)等級(jí)[1],即
完全代謝緩解 (CMR):所有病灶FDG代謝程度均低于肝臟/主動(dòng)脈參考區(qū)且沒有肉眼可見的代謝增高灶,并且與基線檢查相比,沒有新增病灶。
部分代謝緩解 (PMR):與基線檢查相比,病灶SULpeak下降至少30%且SUL絕對(duì)值下降至少0.8。
疾病穩(wěn)定 (SMD):除CMR,PMR及PMD以外的狀態(tài)。
疾病代謝進(jìn)展 (PMD):與基線檢查相比,病灶SULpeak升高至少30%且SUL絕對(duì)值上升至少0.8;或病灶TLG升高75%;或有新增病灶。
根據(jù)以上定義,在實(shí)際操作中,PERCIST標(biāo)準(zhǔn)中主要參數(shù)的推薦測(cè)量方法[2]如下圖所示:

圖1. PERCIST標(biāo)準(zhǔn)中需要測(cè)量的指標(biāo)
其中,主要指標(biāo)有: 正常肝右葉SULmean值(ROI直徑為3cm)及其標(biāo)準(zhǔn)差SD
全身代謝最高病灶的SULpeak值(ROI直徑需≤1.2cm,最多可選5個(gè)病灶,每個(gè)器官最多選2個(gè)病灶)
腫瘤代謝體積 (MTV)
腫瘤負(fù)荷 (TLG)
由以上參數(shù)可以看出,PERCIST標(biāo)準(zhǔn)對(duì)于不同的治療結(jié)果等級(jí)給出了明確的定義,但是同時(shí)也要求大量的定量測(cè)量和指標(biāo)計(jì)算。因此PERCIST標(biāo)準(zhǔn)在實(shí)際的臨床應(yīng)用中還面臨著非常大阻力:
腫瘤的療效分析需要測(cè)量的參數(shù)眾多。尤其是全身多發(fā)轉(zhuǎn)移患者,要同時(shí)測(cè)量全身多個(gè)病灶的眾多定量指標(biāo)。因此常規(guī)執(zhí)行PERCIST標(biāo)準(zhǔn)時(shí)需要很長(zhǎng)的耗時(shí)。
PERCIST標(biāo)準(zhǔn)涉及VOI的勾畫,很多的測(cè)量值(MTV、SULmean、SULpeak和TLG)都會(huì)受到VOI勾畫情況的影響,但是VOI的勾畫很大程度受到人為因素影響,不同醫(yī)生的勾畫結(jié)果往往存在差異,重復(fù)性非常差,這會(huì)進(jìn)一步降低其臨床價(jià)值及適用性。
如何得到一個(gè)標(biāo)準(zhǔn)、可重復(fù)的SUV定量工具,來(lái)對(duì)比評(píng)估腫瘤的代謝情況?
精準(zhǔn)腫瘤自動(dòng)療效評(píng)估平臺(tái)
西門子推出全新的精準(zhǔn)腫瘤自動(dòng)療效評(píng)估平臺(tái),基于PERCIST標(biāo)準(zhǔn),精準(zhǔn)腫瘤自動(dòng)療效評(píng)估平臺(tái)能夠?qū)崿F(xiàn)全流程實(shí)體腫瘤全自動(dòng)測(cè)量、對(duì)比和療效評(píng)估。
西門子獨(dú)家ALPHA人工智能引擎
在分子影像學(xué)中,為了觀察病灶的變化,需要醫(yī)師進(jìn)行多個(gè)時(shí)間點(diǎn)圖像的比較,因此需要圖像之間的同軸配準(zhǔn)。傳統(tǒng)的配準(zhǔn)方法是逐像素進(jìn)行的,然而當(dāng)兩次檢查的視野、患者姿勢(shì)(如:手臂舉起VS手臂放下)或檢查床設(shè)置(如:厚床墊VS薄床墊)發(fā)生變化,傳統(tǒng)算法會(huì)失效,錯(cuò)誤的配準(zhǔn)可能導(dǎo)致病灶消失的假象。
ALPHA基于專利的器官識(shí)別技術(shù)進(jìn)行解剖學(xué)配準(zhǔn),使醫(yī)師更便捷的對(duì)比不同檢查的數(shù)據(jù)。該技術(shù)在每幅圖像中探測(cè)多達(dá)28個(gè)解剖學(xué)標(biāo)識(shí),基于解剖一致性檢查進(jìn)行過(guò)濾,并利用重疊標(biāo)識(shí)對(duì)不同時(shí)間點(diǎn)的圖像進(jìn)行配準(zhǔn)。由于ALPHA配準(zhǔn)是以解剖結(jié)構(gòu)識(shí)別為基礎(chǔ)的,就像人工進(jìn)行圖像配準(zhǔn)一樣,而不是低水平的像素匹配,不受前述所有變化的影響。

圖2: ALPHA配準(zhǔn)可對(duì)多時(shí)間點(diǎn)的檢查圖像進(jìn)行匹配,即使它們有不同的FOV
MFS多病灶自動(dòng)勾畫引擎
MFS根據(jù)PERCIST療效評(píng)估標(biāo)準(zhǔn)的內(nèi)容進(jìn)行閾值及參數(shù)設(shè)置,利用ALPHA算法對(duì)全身高代謝區(qū)域進(jìn)行自動(dòng)勾畫,并自動(dòng)計(jì)算腫瘤代謝體積 (MTV) 、SUL(平均值、極值和峰值)和全身腫瘤負(fù)荷(TLG),方便臨床醫(yī)生完成精準(zhǔn)的療效評(píng)估及預(yù)后評(píng)價(jià)。它能實(shí)現(xiàn):
自動(dòng)勾畫肝臟/主動(dòng)脈參考區(qū)
自動(dòng)配準(zhǔn)不同時(shí)間點(diǎn)檢查中的同一病灶
自動(dòng)勾畫全身高代謝病灶
自動(dòng)計(jì)算單一病灶及全身病灶的MTV及TLG值
使用MFS進(jìn)行全身高代謝區(qū)自動(dòng)勾劃,可減少操作者的主觀依賴性并提高臨床工作效率。研究顯示,當(dāng)計(jì)算骨腫瘤負(fù)荷時(shí),對(duì)于病灶小于6個(gè)的患者,手動(dòng)測(cè)量需要約30分鐘,而使用MFS測(cè)量全身高代謝病灶僅需30秒;對(duì)于6-20個(gè)病灶的患者,手動(dòng)測(cè)量需要約60分鐘,而使用MFS測(cè)量?jī)H需2分鐘;對(duì)于20個(gè)病灶以上的患者,MFS與手動(dòng)測(cè)量的差距更大。
研究結(jié)果指出,與手動(dòng)測(cè)量相比,MFS至少可提升30倍的測(cè)量速度,并且使用MFS測(cè)量的結(jié)果與醫(yī)生手動(dòng)測(cè)量結(jié)果得出的臨床信息相同[3]。MFS功能可提升臨床工作效率并提供精準(zhǔn)、客觀的療效評(píng)估及預(yù)后評(píng)價(jià)所需參數(shù)。為臨床工作及科研提供高效、準(zhǔn)確的解決方案。
準(zhǔn)確的療效評(píng)價(jià)及預(yù)后源自規(guī)范化的測(cè)量方法。根據(jù)指南,對(duì)同一患者進(jìn)行PERCIST標(biāo)準(zhǔn)評(píng)估,需測(cè)量全身所有病灶并選出代謝最高的5個(gè)病灶進(jìn)行計(jì)算。此外,對(duì)于肝臟或主動(dòng)脈區(qū)域的參考值測(cè)量也有相應(yīng)的規(guī)定(VOI直徑為3cm)。MFS會(huì)根據(jù)PERCIST標(biāo)準(zhǔn)的要求自動(dòng)標(biāo)記肝臟或者主動(dòng)脈區(qū)域的參考VOI,并自動(dòng)篩選出用于評(píng)估療效的5個(gè)病灶,根據(jù)這些病灶的多種定量指標(biāo)醫(yī)生可以更為準(zhǔn)確地給出療效評(píng)估等級(jí)(完全代謝緩解、部分代謝緩解、疾病穩(wěn)定、疾病代謝進(jìn)展)。
2019年Mariana R. Camacho的一項(xiàng)研究顯示MFS與手動(dòng)勾畫相比, MTV和TLG具有較好的一致性[4]。該前瞻性研究納入50名經(jīng)病理活檢確認(rèn)的淋巴瘤患者,PET/CT掃描后的圖像分別以20%和40%的閾值進(jìn)行手動(dòng)勾畫和MFS自動(dòng)勾畫獲取VOI,對(duì)兩者得到的MTV和TLG進(jìn)行對(duì)比。

圖3. 手動(dòng)勾畫(A)與MFS自動(dòng)勾畫(B)病灶VOI對(duì)比
對(duì)比結(jié)果顯示兩種勾畫方法得到的MTV和TLG,大部分?jǐn)?shù)據(jù)有較好的一致性,不一致性的數(shù)據(jù)主要出現(xiàn)在MTV和TLG數(shù)值較大的病灶。

圖4. 手動(dòng)勾畫與MFS自動(dòng)勾畫得到的MTV和TLG一致性分析
并且將兩名醫(yī)師使用MFS自動(dòng)勾畫方法得到的MTV和TLG數(shù)據(jù)進(jìn)行對(duì)比分析,顯示兩者均無(wú)顯著性差異。這一研究結(jié)果表明MFS可以快速、可重復(fù)地為臨床提供與手動(dòng)勾畫具有可比性的MTV和TLG數(shù)據(jù)。

圖5. 兩名醫(yī)師使用MFS得到的MTV和TLG差異性分析
MTV和TLG
MFS平臺(tái)除了能夠自動(dòng)勾畫分割全身病灶,還能基于勾畫結(jié)果自動(dòng)計(jì)算腫瘤代謝體積 (MTV) 和全身腫瘤負(fù)荷(TLG),方便臨床醫(yī)生進(jìn)一步完成精準(zhǔn)的療效評(píng)估及預(yù)后評(píng)價(jià)。
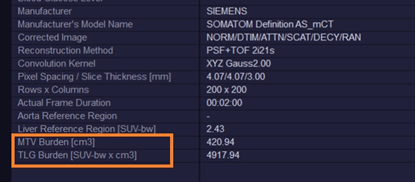
圖6. MFS自動(dòng)計(jì)算MTV及TLG值
腫瘤代謝體積 (MTV)和全身腫瘤負(fù)荷(TLG)是近幾年腫瘤預(yù)后評(píng)價(jià)及治療方案選擇中新興的重要參數(shù)。相對(duì)于單個(gè)病灶,越來(lái)越多的臨床醫(yī)生更傾向于考慮患者全身整體的腫瘤負(fù)荷。此外,單純測(cè)量SUVmax值易受多種因素影響(如患者血糖、注射后間隔時(shí)間及重建方法等),而MTV和TLG相對(duì)于SUVmax,其影響因素少、變異性小,近年來(lái)被大量用于評(píng)估腫瘤患者的預(yù)后情況。
Park等人的研究報(bào)告了在早期非小細(xì)胞肺癌(NSCLC)患者中,治療前PET/CT檢查的TLG值對(duì)患者5年整體生存率(OS)有良好的預(yù)測(cè)價(jià)值[5]。作者指出,應(yīng)密切監(jiān)測(cè)具有高TLG值 (TLG>13.76)患者的復(fù)發(fā)情況,并提示此類患者可從輔助化療中獲益。
同樣,在Lee等人的一項(xiàng)回顧性研究中,作者納入了87名術(shù)前接受FDG PET/CT掃描的胰腺癌患者,探究TLG與MTV對(duì)胰腺癌患者的預(yù)后價(jià)值。研究結(jié)果顯示治療前18F-FDG PET/CT檢查得到的MTV值和TLG值對(duì)胰腺癌患者無(wú)復(fù)發(fā)生存率(RFS)和整體生存率(OS)有良好的預(yù)測(cè)價(jià)值[6]。

圖7. MTV 和TLG 對(duì)胰腺癌患者RFS及OS的預(yù)后價(jià)值