上皮性卵巢癌是最致命的卵巢癌,經常表現為晚期疾病,如腹膜轉移,疾病已擴散到整個腹膜腔。晚期疾病的預后較差,5年總生存率為18% ~ 46%。大多數患者死于廣泛的腹膜疾病負擔和惡性腸梗阻。
紐約威爾康奈爾醫學院放射學系分子成像創新研究所的Sarah M. Cheal博士說:“由于過去幾十年免疫和靶向療法的爆炸式發展,尤其是那些靶向HER2的療法——人們對替代的、更創新的療法治療上皮性卵巢癌的潛在作用越來越感興趣。在這項研究中,我們調整了我們的PRIT系統來靶向上皮性卵巢癌的HER2,并探索它是否可以有效地治療疾病而沒有顯著的毒性。“
臨床前研究包括5組,每組8 ~ 10只裸鼠,每只小鼠均患有腹膜轉移瘤。兩組小鼠分別接受1個或2個周期的anti-HER2225Ac-PRIT治療;其他組接受替代治療或不接受治療,并作為對照。每周監測體重和腫瘤進展長達154天。
腫瘤在未經治療的小鼠中迅速擴散,導致中位生存期約為4個月。然而,當接受1個或2個周期的anti-HER2225Ac-PRIT治療時,154天后未達到中位生存期。在研究結束時,anti-HER2 225Ac-PRIT治療組中75%的小鼠被證實臨床治愈。小鼠對所有治療均耐受良好。
紐約紀念斯隆·凱特琳癌癥中心放射科的醫學博士Steven M. Larson說:”在這項研究中,我們使用anti-HER2225Ac-PRIT實現了高效力,同時保持了可接受的安全性。這些研究結果表明,當擴展到人類患者時,我們可以達到治愈腫瘤的輻射吸收劑量,而沒有主要的正常器官毒性。”
紐約紀念斯隆·凱特琳癌癥中心兒科部的Nai-Kong V. Cheung博士說:“此外,由于基于DOTA的PRIT是模塊化的,它可以適用于其他癌癥和使用SADA(自組裝分解抗體)的下一代PRIT,具有潛在廣泛應用于腫瘤的室間(如腹膜)和全身治療。”
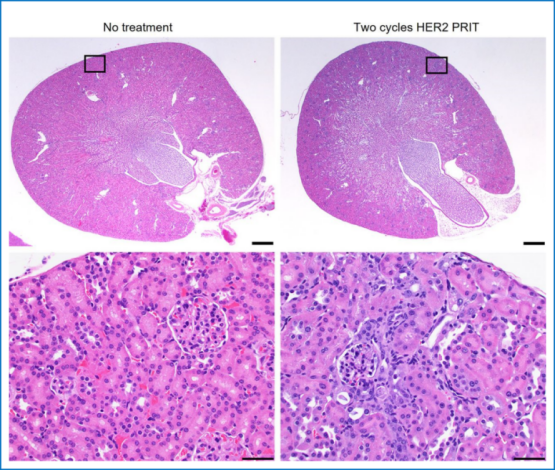
圖5。接受1個 (37 kBq)或2個 (74 kBq)周期的HER2 225Ac-PRIT治療的小鼠中觀察到最小到輕度的放射性腎病。如圖所示,在腫瘤接種后154天(治療開始于第15天),未經治療的對照組和接受2個周期的HER2 225Ac-PRITT治療的小鼠腎臟的代表性蘇木精和伊紅染色。頂部圖像的比例尺:500μm。底部圖像的比例尺:50μm。