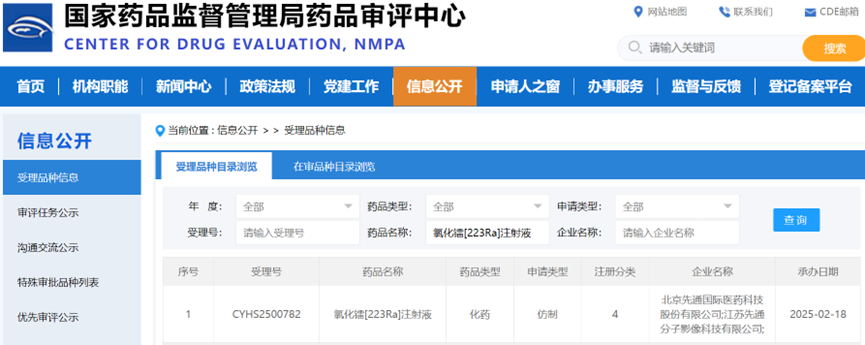
2月18日,北京先通國際醫藥科技股份有限公司(先通醫藥)研發的4類(境內仿制藥)放射性治療藥物氯化鐳[223Ra]注射液的申報生產申請獲國家藥品監督管理局藥品審評中心受理公開。2020年8月27日,國家藥品監督管理局(NMPA)批準了拜耳公司的氯化鐳[223Ra]注射液(商品名:多菲戈®或Xofigo®)在國內上市,用于治療伴癥狀性骨轉移且無已知內臟轉移的去勢抵抗性前列腺癌(CRPC)患者。
不同傳統癌癥治療藥物,Xofigo®有著獨特的抗癌方式。我們知道,癌癥發展到一定階段,腫瘤細胞會發生轉移,而骨轉移是許多癌癥患者面臨的嚴重問題,尤其是前列腺癌患者,骨轉移的發生率相當高。Xofigo®的活性部分巧妙地模擬了鈣離子,憑借這一特性,它能夠與骨骼中的羥基磷灰石形成復合物,從而具有了親骨性,特別傾向于聚集在骨轉移病理骨增生活躍的區域。
一旦定位到骨轉移區域,Xofigo®便開始發揮它強大的抗癌作用。Xofigo®是一種靶向α粒子放射性治療藥物,不同于發射β粒子的放射性核素,223Ra屬于高LET射線,發射α粒子可在短距離內(<100微米)引發腫瘤細胞DNA雙鏈斷裂,產生強效的細胞毒性作用,同時減少對周圍正常組織的損傷,且這種雙鏈損壞很難被修復,這與β粒子造成的單鏈DNA斷裂相比具有明顯優勢。
Xofigo®在臨床應用中得到充分的驗證,多項臨床研究數據證明了Xofigo®的卓越療效。關鍵性III期ALSYMPCA 研究堪稱這一領域的經典研究,它為Xofigo®的療效提供了堅實的證據。在這項研究中,研究人員將Xofigo®與安慰劑進行了嚴格的對比試驗。結果顯示,使用Xofigo®治療的患者,總生存期(OS)得到了顯著改善。具體數據表明,與安慰劑組相比,接受Xofigo®治療的患者中位總生存期明顯延長,這意味著更多患者能夠在治療后生存更長時間,為他們爭取到了寶貴的生命時光。
同時,Xofigo®在延遲首次癥狀性骨骼事件(SSE)的發生時間方面也表現出色。骨轉移常常會導致一系列嚴重的骨骼事件,如病理性骨折、脊髓壓迫等,這些事件不僅會給患者帶來巨大的痛苦,還會嚴重影響患者的生活質量和預后。而ALSYMPCA研究數據顯示,使用Xofigo®治療的患者,首次癥狀性骨骼事件的發生時間得到了顯著延遲 ,這大大降低了患者發生嚴重骨骼并發癥的風險,讓患者在更長時間內保持相對較好的身體狀態,減少了因骨骼事件帶來的痛苦和生活不便,顯著提高了患者的生活質量。
氯化鐳[223Ra]注射液:潛力無限的市場價值
從全球范圍來看,放射性藥物市場近年來呈現出迅猛的增長態勢,已然成為醫藥領域中一顆耀眼的新星。隨著科技的不斷進步以及人們對健康關注度的日益提高,放射性藥物在疾病診斷與治療領域的應用愈發廣泛,市場規模也隨之持續擴張。
根據BCC Research數據,2020年全球核藥市場規模達到93億美元,預計2021-2026年市場年均復合增速為11.0%,2026年市場整體規模將達到175億美元。而在2024-2029年的預測期內,全球核醫藥市場預計將從126億美元增長到210億美元,復合年增長率(CAGR)為 8.29%。這一增長趨勢背后,是多種因素共同作用的結果。全球人口老齡化進程的加速,使得與年齡相關的疾病,如癌癥、心血管疾病等的發病率不斷上升,對放射性藥物的需求也隨之水漲船高。
在這樣蓬勃發展的大市場中,氯化鐳[223Ra]注射液憑借其獨特的治療優勢和顯著的臨床效果,占據了重要的市場地位,展現出巨大的市場潛力。自2013年獲批上市以來,Xofigo®在全球范圍內的銷售額逐年攀升,2017年其全球銷售額達到4.08億歐元,成為了癌癥治療領域的明星產品。這一成績的取得,充分證明了Xofigo®在市場上的受歡迎程度和認可度。
從市場需求角度來看,Xofigo®的目標患者群體規模龐大。前列腺癌作為男性泌尿生殖系統中最為常見的腫瘤之一,近年來其發病率在全球范圍內呈現出上升趨勢。據國際癌癥研究機構(IARC)發布的數據顯示,2020年全球前列腺癌新發病例數高達141萬,占癌癥新發病例總數的7.3%。隨著人口老齡化的加劇,這一數字預計還將持續增長。而在前列腺癌患者中,相當一部分會發展為去勢抵抗性前列腺癌,并出現骨轉移,這些患者都有可能成為Xofigo®的潛在使用者。龐大的患者群體為Xofigo®提供了廣闊的市場空間,也為國內核藥企業研發該產品奠定了堅實的市場基礎。
氯化鐳[223Ra]注射液:機遇與挑戰并存
目前,國內的氯化鐳[223Ra]注射液市場主要依賴進口,Xofigo®于2020年獲批進入中國市場,為國內患者帶來了新的治療選擇。然而,進口藥物往往伴隨著較高的價格,據了解,Xofigo®參考價格約一針4萬元,每4周注射1次,全療程共計注射6 次。且目前尚未進入醫保,這無疑給患者帶來了沉重的經濟負擔,使得許多患者望而卻步,限制了藥物的可及性。
不過,值得欣喜的是,國內眾多核藥企業已經敏銳地捕捉到了這一市場需求和發展機遇,紛紛加大在氯化鐳[223Ra]注射液研發方面的投入和布局。像先通醫藥等國內知名核藥企業,憑借著自身強大的研發實力和資源優勢,積極投身于相關研發項目中。它們在放射性藥物研發領域不斷探索創新,致力于突破技術瓶頸,研發出具有自主知識產權的氯化鐳[223Ra]注射液,以實現該藥物的國產化替代,降低患者的治療成本。
但不可否認的是,國內核藥企業在研發氯化鐳[223Ra]注射液的道路上,仍面臨著諸多嚴峻的挑戰。從技術層面來看,放射性藥物的研發涉及到核物理、放射化學、藥學、醫學等多個學科領域,技術門檻極高。研發過程中需要精確控制放射性核素的制備、標記、純化等關鍵環節,確保藥物的安全性、有效性和穩定性,每一個環節都充滿了技術難題,需要大量的科研人員和先進的實驗設備進行深入研究和反復驗證。
資金方面,研發一款新藥需要巨額的資金投入,從前期的基礎研究、臨床前研究,到臨床試驗的各個階段,再到最終的藥品上市,整個過程需要耗費大量的資金。而且,新藥研發周期長,不確定性高,一旦研發失敗,企業將面臨巨大的經濟損失。這對于許多企業來說,是一個巨大的資金壓力和風險挑戰。
人才短缺也是制約國內核藥企業研發的重要因素之一。由于放射性藥物研發的專業性和復雜性,需要既懂核技術又懂醫藥研發的復合型人才。然而,目前國內相關專業人才培養體系尚不完善,人才儲備相對不足,難以滿足企業快速發展的研發需求。企業在吸引和留住這些專業人才方面也面臨著激烈的競爭,進一步增加了研發的難度。
國內核藥企業研發氯化鐳[223Ra]注射液,從滿足國內醫療需求、打破國外壟斷等多方面具有不可忽視的價值和深遠意義。若國內核藥企業成功研發氯化鐳[223Ra]注射液,那將在國內市場掀起巨大的波瀾。從市場層面來看,這不僅能夠顯著提升藥物的可及性,讓更多患者能夠及時用上這種有效的治療藥物,還能通過市場競爭機制,進一步降低藥物價格,使更多患者受益。而且,國產化的氯化鐳[223Ra]注射液有望借助國內完善的醫藥產業鏈和強大的生產能力,實現規模化生產,從而更好地滿足國內市場的需求,提升我國核藥產業的國際影響力。