近期,中南大學(xué)湘雅醫(yī)院核醫(yī)學(xué)科(PET中心)/國(guó)家衛(wèi)健委納米生物技術(shù)重點(diǎn)實(shí)驗(yàn)室主任胡碩教授團(tuán)隊(duì)分別在《Advanced Science》雜志(中科院1區(qū)Top期刊,IF=14.3)和《Biomaterials》(中科院1區(qū)Top期刊,IF=12.8)發(fā)表題為《Biomineralized Nanocomposite-Integrated Microneedle Patch for Combined Brachytherapy and Photothermal Therapy in Postoperative Melanoma Recurrence and Infectious Wound Healing》和《A177Lu-nucleotide Coordination Polymer-incorporated Thermosensitive Hydrogel with Anti-inflammatory and Chondroprotective Capabilities for Osteoarthritis Treatment》的原創(chuàng)性研究。國(guó)家衛(wèi)健委納米生物技術(shù)重點(diǎn)實(shí)驗(yàn)室劉鵬副研究員和核醫(yī)學(xué)科(PET中心)郝璐博士為前一篇論文的共同第一作者,胡碩教授和美國(guó)威斯康星大學(xué)蔡偉波教授為共同通訊作者。劉鵬副研究員和核醫(yī)學(xué)科(PET中心)副主任技師周明為后一篇論文的共同第一作者,胡碩教授和湘雅藥學(xué)院周文虎教授為共同通訊作者,中南大學(xué)湘雅醫(yī)院為兩篇論文的第一單位和第一通訊單位。
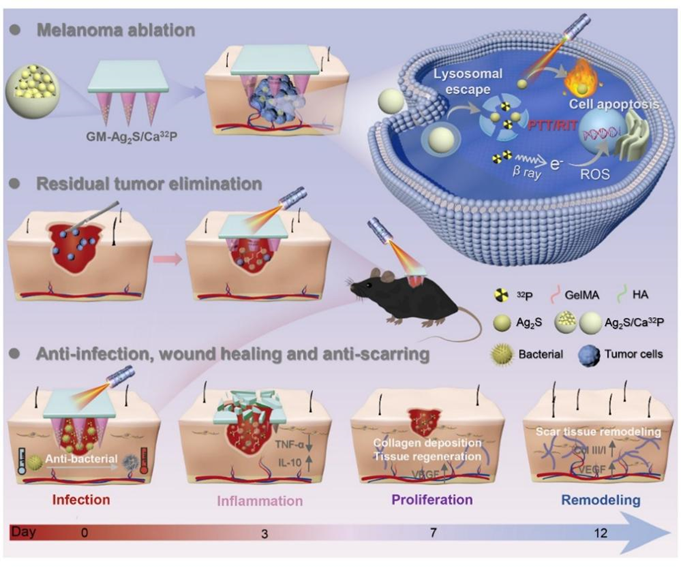
《Biomineralized Nanocomposite-Integrated Microneedle Patch for Combined Brachytherapy and Photothermal Therapy in Postoperative Melanoma Recurrence and Infectious Wound Healing》研究中設(shè)計(jì)了一種多功能納米復(fù)合微針貼片,通過近距離放療和光熱治療協(xié)同抑制黑色素瘤術(shù)后復(fù)發(fā)和感染,并通過促進(jìn)肉芽組織新生、膠原蛋白沉積和血管生成來促進(jìn)無瘢痕的傷口愈合。
黑色素瘤是一種高度侵襲性的起源于皮膚黑色素細(xì)胞的惡性腫瘤。目前,早期黑色素瘤以手術(shù)干預(yù)為主,然而,受發(fā)病部位、不完全手術(shù)切除等的限制,剩余無癥狀但已出現(xiàn)浸潤(rùn)的腫瘤組織不可避免地會(huì)引發(fā)腫瘤復(fù)發(fā)或遠(yuǎn)處轉(zhuǎn)移。此外,由于腫瘤病人惡病質(zhì)導(dǎo)致的免疫力低下,加之全層皮膚缺損和手術(shù)后較大開放性損傷,傷口感染或慢性炎性傷口形成的風(fēng)險(xiǎn)顯著增加。因此,迫切需要一種有效去除殘留浸潤(rùn)性腫瘤細(xì)胞、抑制感染和加速傷口修復(fù)的治療方法來提高惡性腫瘤患者的生存率和生活質(zhì)量。該團(tuán)隊(duì)開發(fā)了一種多功能納米復(fù)合微針貼片,使用微針平臺(tái)將近距離放療和光熱治療相結(jié)合,從而為術(shù)后黑色素瘤復(fù)發(fā)和感染傷口愈合提供輔助治療。這種微針貼片可穿透皮下組織,向浸潤(rùn)的腫瘤細(xì)胞和感染部位的細(xì)菌遞送治療藥物,進(jìn)而實(shí)現(xiàn)腫瘤細(xì)胞和細(xì)菌的清除。此外,該納米復(fù)合微針貼片還可通過減少炎癥和促進(jìn)肉芽組織形成、膠原沉積和血管生成來促進(jìn)無疤痕傷口愈合。本研究構(gòu)建的微針遞送系統(tǒng)為黑色素瘤術(shù)后復(fù)發(fā)和感染提供了新的思路,顯示出在臨床術(shù)后應(yīng)用中的巨大前景。

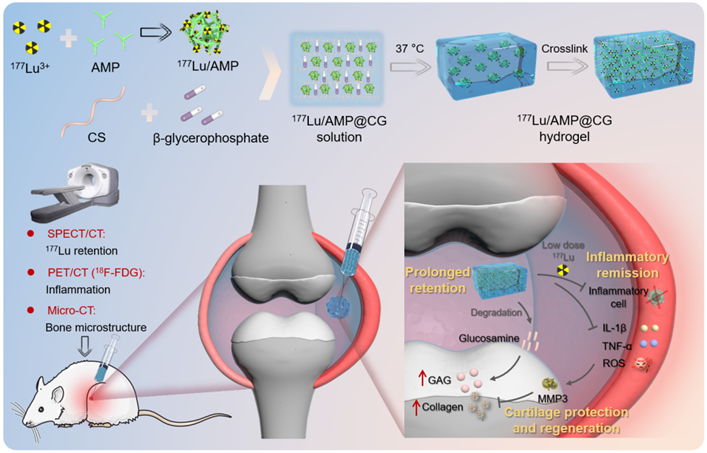
《A177Lu-nucleotide Coordination Polymer-incorporated Thermosensitive Hydrogel with Anti-inflammatory and Chondroprotective Capabilities for Osteoarthritis Treatment》研究中利用放射性同位素177Lu與單磷酸腺苷形成金屬有機(jī)配位聚合物,并將其嵌入由殼聚糖/β-甘油磷酸鹽組成的溫敏水凝膠中,構(gòu)建177Lu/AMP@CG復(fù)合凝膠。該復(fù)合凝膠展現(xiàn)了優(yōu)異的抗炎、軟骨修復(fù)及保護(hù)性能,為骨關(guān)節(jié)炎提供了一種安全有效的治療策略。
骨關(guān)節(jié)炎(OA)是一種以關(guān)節(jié)軟骨損傷和滑膜炎癥為主要特征的慢性疾病,其發(fā)病機(jī)制尚不明確,且臨床上缺乏有效的治療手段。放射性滑膜切除術(shù)(RSO)通過放射性核素內(nèi)照射作用可抑制滑膜炎癥并減少軟骨破壞,在OA等關(guān)節(jié)炎性疾病的治療中展現(xiàn)出顯著的療效,但受限于放射性同位素的毒性和清除問題。本文提出了一種關(guān)節(jié)腔注射溫敏凝膠策略,利用放射性同位素177Lu與單磷酸腺苷(AMP)構(gòu)建金屬有機(jī)配位聚合物(MCPs),并將MCPs嵌入殼聚糖/β-甘油磷酸鹽(CG)溫敏水凝膠中構(gòu)建177Lu/AMP@CG復(fù)合凝膠。177Lu/AMP@CG利用納米框架和溫敏凝膠的“雙重屏障”作用實(shí)現(xiàn)核素的關(guān)節(jié)腔有效滯留,并通過低劑量核素長(zhǎng)時(shí)內(nèi)照射抑制滑膜炎癥,殼聚糖溫敏凝膠可發(fā)揮緩沖和修復(fù)軟骨的作用,雙管齊下實(shí)現(xiàn)高效安全的OA治療。本研究為關(guān)節(jié)腔注射放射性核素制劑的研究和開發(fā)提供參考,為OA 的治療研究提供新的思路。