在過去25年中,由于技術(shù)的進(jìn)步和對(duì)如何利用放射生物學(xué)遠(yuǎn)離的更好理解,放射腫瘤學(xué)領(lǐng)域發(fā)生了重大變化。改變分割模式、即改變每次治療的輻射劑量,以及治療的頻率,包括每天多次劑量的照射,已經(jīng)成為一種常見的方案。化學(xué)治療與放射治療相結(jié)合,無論是序貫還是同步,也已成為眾多部位疾病的標(biāo)準(zhǔn)治療方法。以下部分將簡(jiǎn)要回顧一些放射治療的技術(shù)進(jìn)展。
一、調(diào)強(qiáng)放射治療
傳統(tǒng)上,當(dāng)使用外照射放射治療時(shí),首先要考慮到腫瘤的位置和周圍的正常組織結(jié)構(gòu)來確定放射治療技術(shù),然后選擇要使用的射束的方向、能量和數(shù)量以保障靶體積最佳覆蓋照射同時(shí)相鄰正常組織結(jié)構(gòu)受照射最少。這種方法的劑量分布是通過改變射野的大小或權(quán)重,添加射野擋塊或添加其他諸如組織補(bǔ)償器之類的裝置(如楔形板等)重新分布能量來保護(hù)正常組織結(jié)構(gòu)。這就是所謂的正向治療計(jì)劃。
最近,利用計(jì)算機(jī)技術(shù)和設(shè)備工程的進(jìn)步,開發(fā)了一種不同的方式稱為逆向治療計(jì)劃。在這里,放射腫瘤醫(yī)師在制定治療方案時(shí)要首先設(shè)置靶組織及正常器官的劑量參數(shù)。每個(gè)勾畫對(duì)象都有優(yōu)先權(quán)或等級(jí)順序。計(jì)算機(jī)程序可以不斷優(yōu)化放射治療計(jì)劃以達(dá)到預(yù)期目標(biāo)。考慮多種可能性并評(píng)估許多迭代次數(shù)。這種評(píng)估通過使用劑量一體積直方圖分析來優(yōu)化,其可以將正常危及組織器官所受輻射劑量進(jìn)行量化。只有在找到可接受的放射劑量分布后,才能最終確定使用哪一種技術(shù)。
調(diào)強(qiáng)放射治療(IMRT)可以通過一步一拍(靜態(tài)MRT)或滑動(dòng)窗口技術(shù)(動(dòng)態(tài)MRT)來實(shí)現(xiàn)。在靜態(tài)調(diào)強(qiáng)方法中,在多葉光柵(MLC)調(diào)整其正確的形狀時(shí),加速器停止出束,而在后一種方法中,MLC調(diào)整過程中加速器持續(xù)出束。IMRT計(jì)劃高度適用于危及器官的最佳保留,特別是凹形靶區(qū)的覆蓋。然而,IMRT計(jì)劃往往有更高的總監(jiān)控裝置(MUs),并增加對(duì)周圍組織的低劑量照射。
IMRT的延伸是容積弧形調(diào)強(qiáng)放射治療(VMAT),它將機(jī)架旋轉(zhuǎn)/動(dòng)態(tài)MLC運(yùn)動(dòng)和劑量率的變化相結(jié)合以創(chuàng)造高度適形放射治療劑量分布。VMAT計(jì)劃可以使用單個(gè)360°弧線或多個(gè)弧線進(jìn)行治療,也可以采用螺旋狀,類似CT的輸送方式。VMAT相對(duì)于傳統(tǒng)IMRT的主要優(yōu)點(diǎn)是減少了治療時(shí)間,同時(shí)累積劑量也可能下降;對(duì)于高度復(fù)雜的靶目標(biāo),其也有可能產(chǎn)生更大的腫瘤劑量適形性。

二、 圖像引導(dǎo)放射治療
從計(jì)劃階段轉(zhuǎn)向治療需要精確地實(shí)施所選擇的治療技術(shù)。在首先確認(rèn)患者在模擬定位過程中創(chuàng)建的支撐平臺(tái)內(nèi)的位置是正確的之后,可以通過幾種方式來實(shí)現(xiàn)。盡管大多數(shù)患者接受更深層次位置的放射治療,但在治療皮膚或淺表惡性腫瘤的情況下可以直接觀察淺表腫瘤的臨床變化。每個(gè)射野或光東的平片圖像已經(jīng)使用幾十年,在這里,隨著技術(shù)的進(jìn)步,診斷成像已經(jīng)融合到治療中,使得治療可以基于在患者處于治療位置時(shí)獲得的CT掃描。放射腫瘤醫(yī)師可以利用兆伏級(jí)或錐形東CT掃描直觀地顯示靶目標(biāo),根據(jù)靶目標(biāo)當(dāng)前的位置進(jìn)行調(diào)整,然而也需要考慮相鄰的正常結(jié)構(gòu)組織。放置在腫瘤內(nèi)或附近的替代物(例如基準(zhǔn)標(biāo)記物)可用于評(píng)估放射治療的聚焦點(diǎn)。其他系統(tǒng)包括(但不限于)超聲引導(dǎo)成像、三維光學(xué)表面監(jiān)測(cè)、紅外線或光學(xué)標(biāo)記物追蹤,以及射頻一信標(biāo)引導(dǎo)模式。因此圖像引導(dǎo)放射治療(IGRT)是放射治療期間使用實(shí)時(shí)成像進(jìn)行治療定位。
從IGRT收集的信息可以用來修改治療計(jì)劃。在典型的6周治療過程中,腫瘤體積、患者解剖結(jié)構(gòu)和患者體位的改變會(huì)顯著影響靶目標(biāo)和危及器官的位置和體積。因此,圖像引導(dǎo)可以幫助識(shí)別患者治療時(shí)的那些變化,這可能導(dǎo)致重新做計(jì)劃,重新模擬定位,或兩者都需要。這個(gè)過程稱為自適應(yīng)放射治療,是指根據(jù)解剖變化調(diào)整放射治療。自適應(yīng)放射治療可以與功能成像結(jié)合,例如F- FDG PET,以區(qū)別提高殘存腫瘤或放射抗拒的腫區(qū)域的照射劑量。后一種技術(shù)被稱為劑量繪畫(DP)放射治療。IGRT結(jié)合自適應(yīng)放射治療聯(lián)合使用,可使劑量加至靶目標(biāo),同時(shí)保護(hù)了危及器官。
三、立體定向放射外科/立體定向放射治療
1951年,瑞典神經(jīng)外科醫(yī)生 Lars Leskell首先提出了高劑量放射治療腦病變的概念。立體定向放射外科(SRS)提供了一個(gè)每分次大劑量(通常是單次或3~5次)治療局灶性腦病變,由于其劑量梯度跌落極快,故最大限度地減少了對(duì)周圍正常組織的毒性。最近,立體定向放射治療(SBRT)是SRS的延伸,其通過圖像實(shí)時(shí)引導(dǎo)用于治療顱外轉(zhuǎn)移灶。SBRT可用于治療肺、脊柱、肝臟、胰腺、腎臟和前列腺的局灶性病變。
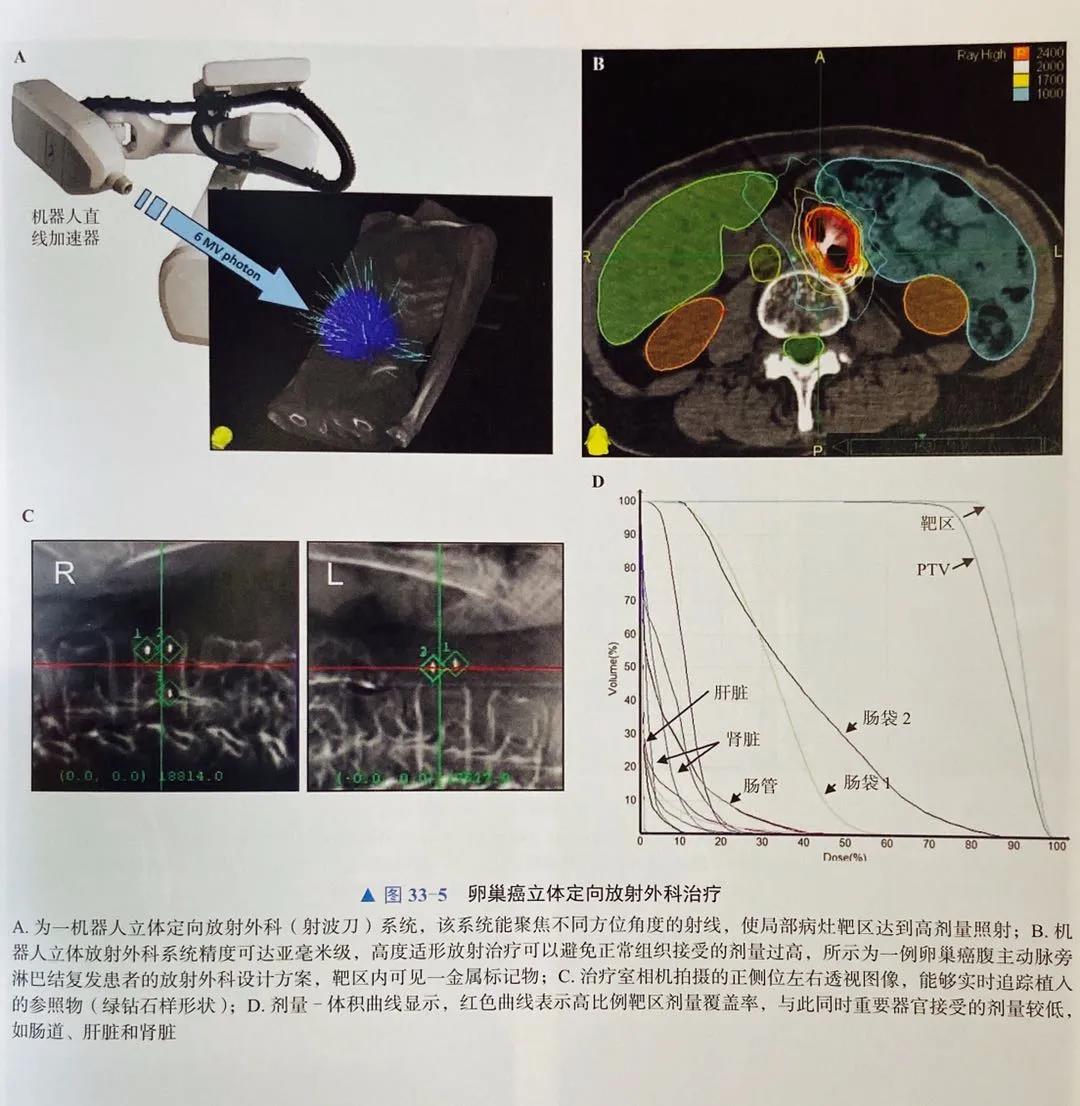
四、粒子束放射治療
雖然放射治疔通常使用不帶電荷的能量稱為光子,但它也可以給出帶電粒子如電子或質(zhì)子或不帶電粒子如中子。這些粒子在物理性質(zhì)上有著不同的優(yōu)勢(shì),因此它們?cè)诮M織中的分布及生物有效性也不同。
在質(zhì)子治療中,主要優(yōu)勢(shì)在于空間分布,能給周圍有需要保護(hù)的區(qū)域提供高劑量照射。當(dāng)考慮到腫瘤接近劑量限制性器官組織如眼睛、大腦和脊髓時(shí),質(zhì)子治療優(yōu)勢(shì)最明顯。使用質(zhì)子,目標(biāo)區(qū)域之外也會(huì)有小的照射劑量。碳離子可以提供類似的劑量梯度和提高生物有效性。重要的是,了解這些放射治療方式的專業(yè)知識(shí)是必要的,因?yàn)樵黾拥倪m形性同時(shí)會(huì)帶來丟失靶目標(biāo)的風(fēng)險(xiǎn)。也就是說,保護(hù)正常組織結(jié)構(gòu)會(huì)增加惡性腫瘤覆蓋率不足的風(fēng)險(xiǎn)。另一條原則是:“如果你沒有擊中你需要擊中的東西,就不要錯(cuò)過你原本想錯(cuò)過的東西。”
中子有助于治療生長(zhǎng)緩慢的腫瘤。它們不像其他粒子那樣具有空間優(yōu)勢(shì),但是它們的放射生物學(xué)效應(yīng)更大,并且在治療放射治療抗拒的腫瘤時(shí)是有利的。缺乏空間優(yōu)勢(shì)導(dǎo)致臨床澘力有限,因?yàn)殡y以向腫瘤提供足夠的劑量,也不會(huì)對(duì)鄰近組織結(jié)構(gòu)帶來潛在的風(fēng)險(xiǎn)。解決這一問題的方法之一是使用硼中子俘獲治療(BNCT)。為此含硼化合物優(yōu)先集中在腫瘤內(nèi),隨后用中子照射瘤。中子與硼的相互作用導(dǎo)致a粒子(重的帶正電的粒子)和鋰核的釋放。它們都具有非常短的輻射范圍,因此可以優(yōu)先與緊鄰的細(xì)胞相互作用,對(duì)腫瘤造成顯著的損傷。這種類型的治療已被用于惡性腦腫瘤。

五、近距離放射治療
近距離放射治療或短程治療被定義為在腫瘤附近放置密封放射源。歷史上最初使用鐳作放射源,但現(xiàn)在使用更安全并具有更多實(shí)際特性的源如碘、鈀、銥和銫。近距離放射治療有三種形式:①第一種類型是將模具或敷貼器置于淺表病變的皮膚或粘膜上;例如,眼敷貼器已被用于治療視母細(xì)胞瘤、眼部黑色素瘤和翼狀胬肉;②組織間插植是將含有放射源或粒子的導(dǎo)管置于軟組織內(nèi),例如前列腺組織間插植;③腔內(nèi)照射是將放射源放置在體腔中,例如陰道近距離放射治療往往用于子宮內(nèi)膜癌的輔助治療。
六、術(shù)中放射治療
術(shù)中放射治療(IORT)技術(shù)在過去的30年中一直存在,但近年來該技術(shù)已經(jīng)越來越受歡迎。這部分歸功于TARGIT-A試驗(yàn)的成功,這是一項(xiàng)國際多中心、隨機(jī)、前瞻性的Ⅲ期非劣效性試驗(yàn),將早期乳腺癌患者被隨機(jī)分配到全乳放射治療和對(duì)瘤床進(jìn)行靶向的IORT,使用低能量X線(kV范圍內(nèi))。
IORT在麻醉狀態(tài)下腫瘤(原發(fā)或復(fù)發(fā))切除后對(duì)瘤床開始照射。IORT的理論優(yōu)勢(shì)是通過最大限度地保護(hù)/屏蔽正常組織并向瘤床實(shí)施大劑量單次照射以改善局部控制而獲得較高的治療比。IORT可作為單一治療,但更常用于聯(lián)合外照射治療(±化學(xué)治療)。目前,市場(chǎng)上存在使用電子、低kV級(jí)光子和192Ir高劑量率的術(shù)中機(jī)器。
七、非密封源
幾十年來,未密封的放射性同位素被用于治療惡性腫瘤。在這種類型的治療中,放射性藥物可口服或靜脈給予患者,如32P、131I、90Y、89Sr和153Sm,它們產(chǎn)生β射線殺傷腫瘤細(xì)胞。盡管第一種放射性藥物通常具有在靶器官或部位累積的內(nèi)在傾向,但是由于它們的血液學(xué)毒性,其使用潛力有限。最近,新一輪的研究導(dǎo)致了生物分子靶向藥物的進(jìn)展,其通過操縱免疫系統(tǒng)來優(yōu)化細(xì)胞毒性劑向特定類型的體細(xì)胞遞送。
八、熱療
對(duì)放射治療來講,熱療可使放射治療增敏。這種作用機(jī)制是多因素的,可能與細(xì)胞存活所必需的DNA修復(fù)蛋白的失活有關(guān)。熱療也是放射治療的補(bǔ)充,因?yàn)榧?xì)胞周期的S期(通常是相對(duì)抗輻射的時(shí)期)對(duì)高溫敏感。另外,缺氧細(xì)胞(相對(duì)抗輻射的)也是熱敏感的,因?yàn)闋I養(yǎng)缺乏的細(xì)胞處于不利于其生長(zhǎng)的酸性pH中。不知道熱療和放射治療的組合是否具有協(xié)同效應(yīng)或相加效應(yīng)。無論如何,這種治療方法可能是治療淺表腫瘤如局部復(fù)發(fā)性乳腺癌的有效方法。從歷史上看,技術(shù)上的局限性使深層腫瘤難以加熱。然而,荷蘭的一項(xiàng)隨機(jī)試驗(yàn)比較了有或沒有深部熱療的放射治療,結(jié)果顯示后者的完全緩解率顯著提高,并帶來生存獲益。新一代的深度熱療設(shè)備加上體內(nèi)磁共振成像(MRI)來提供精確的溫度測(cè)量,此種組合或許有前景。
本文內(nèi)容節(jié)選自《臨床放射腫瘤學(xué): 適應(yīng)證、技術(shù)與療效》,一部高度實(shí)用、基于放射腫瘤生物學(xué)和放射治療臨床療效的綜合性著作。