
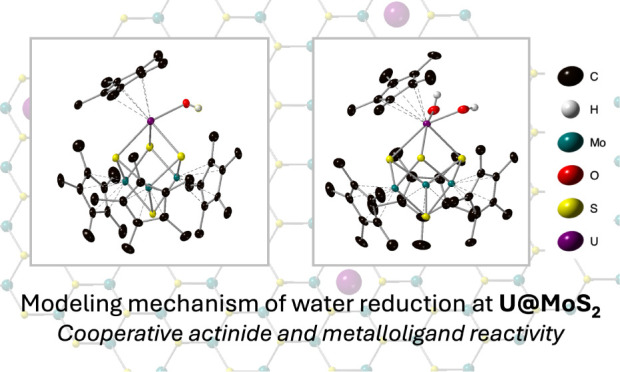
Matson教授團隊聚焦于鈾(U)在水還原反應中的作用機制,通過分子模型研究了鈾原子在二硫化鉬(MoS2)表面上的分散狀態,成功揭示了其在水還原反應中的協同機制。通過合成一系列鈾配合物作為模型,成功分離并表征了U-氫氧化物中間體,深入探究其反應路徑,揭示鈾與金屬配體協同作用于水活化過程,同時對U-O代類似物的形成及穩定性進行研究,為理解鈾在MoS?表面催化水還原反應提供關鍵原子層面視角,助力鈾基催化劑研究發展。該工作由Kamaless Patra, William W. Brennessel, 和 Ellen M. Matson共同撰寫,以“Molecular Models of Atomically Dispersed Uranium at MoS2 Surfaces Reveal Cooperative Mechanism of Water Reduction”為題,發表在《JACS》上。
背景介紹
鈾在核燃料循環中是重要元素,其能呈現多種氧化態(U²?、U³?、U??、U??、U??),5f與6d軌道雜化賦予其豐富氧化還原化學性質,在多電子分子轉化反應中極具潛力。歷史上,早在1909年Haber就曾用鈾作氨合成非均相催化劑,后續貧鈾氧化物也用于氧化反應。近年,原子分散鈾中心錨定在氧化還原活性表面的單原子催化劑(SACs)成為研究熱點,如鈾SACs在氮摻雜碳上用于電化學氮還原制氨、在MoS?納米片上用于電催化析氫等,但這些催化過程的中間體和機制多依賴理論預測,缺乏實驗驗證。
研究出發點
受到鈾SACs在MoS?納米片上用于電催化析氫啟發,發現鈾在氧化還原活性表面獨特反應性及現有研究對其催化機制理解的不足,作者所在團隊旨在利用半立方烷硫代鉬酸鹽簇((Cp*?Mo?S?))與低價鈾的配合物,模擬MoS?基底平面上低價鈾離子,探究其在水活化過程中的反應機制,填補實驗空白,為鈾基催化劑應用提供理論支撐。
圖文解析
要點1:水與鈾配合物反應研究。作者研究了低價鈾氫氧化物形成 。首先研究了作者先前報道的還原鈾簇(Cp*3Mo3S4)Cp*U(1)與水的反應性,將該化合物作為沉積在MoS2納米片(U@MoS2)基面上的單個U原子的分子類似物。再向該化合物的苯溶液中加入一定當量的水,形成鈾-羥基簇合物(Cp*3Mo3S4)Cp*U(OH)。最后向鈾-羥基簇合物中加等量水,在非配位溶劑中生成新產物(Cp?Mo?S?)CpU (OH)?。
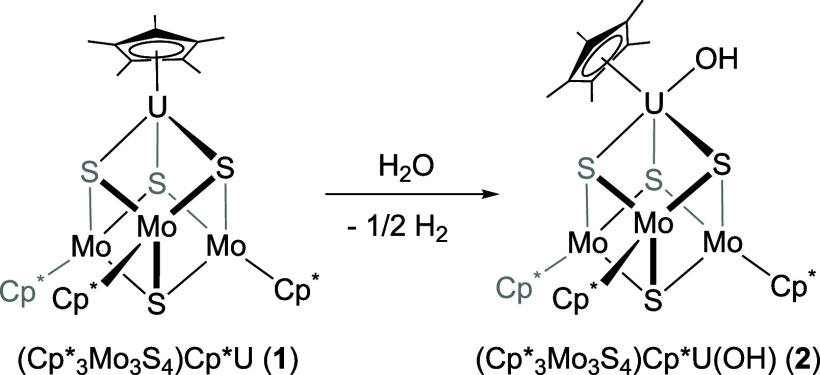
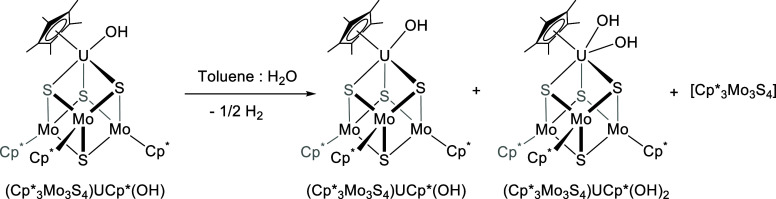
圖1.一價鈾氫氧化物形成。
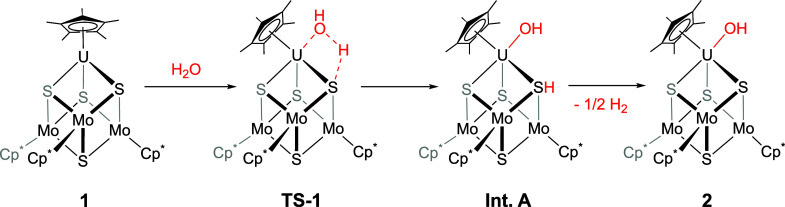
圖2.二價鈾氫氧化物形成。
要點 2 :提出水活化機制 。水的O-H鍵在U-S相互作用下均裂,羥基自由基加至鈾,氫原子加至硫形成中間體A,A中S···H鍵均裂,氫原子結合生成H?和最終產物。通過DFT支持此機制,表明 MoS?邊緣硫中心在氫原子捕獲等過程更具活性,影響析氫反應。同時,對比研究含不同配體的鈾配合物與水反應,凸顯硫代鉬酸鹽金屬配體在水O-H鍵活化中的關鍵作用。

圖3.水活化機制研究。
要點 3 :鈾 -氧代配合物合成研究。研究2與氫原子轉移試劑Gomberg’s dimer反應,溶液變色,¹H NMR 顯示試劑消耗并生成 Ph?CH,推測形成鈾-氧代復合物 [(Cp?Mo?S?)UCp(=O)](4),但4極不穩定。用苯乙烯氧化物進行氧原子轉移反應也得到類似4的產物證據,但因4不穩定,進一步用等電子模型配合物 (Cp?Mo?S?)CpU (=NMes)(5)研究。
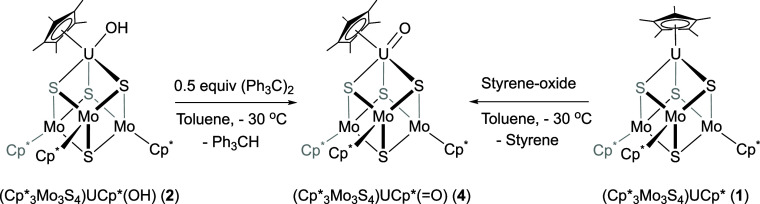
圖4.(Cp*3Mo3S4)Cp*U(=O) (4)的合成。
要點4 :鈾 -氧代配合物結構與穩定性分析。5由1與mesityl azide反應制得,產率近94%。¹H NMR和單晶X射線衍射表征顯示其結構中鈾中心配位環境包含 mesityl imido 取代基、η? - Cp * 配體和硫代鉬酸鹽簇的三個硫原子,U-N鍵長 2.019 (7) Å 具雙鍵特征。通過對比5與2的鍵參數,發現4中鈾-氧鍵可能較弱,解釋了其不穩定原因,表明在該體系中鈾 - 氧代物種作為水活化途徑中間體可能性低。
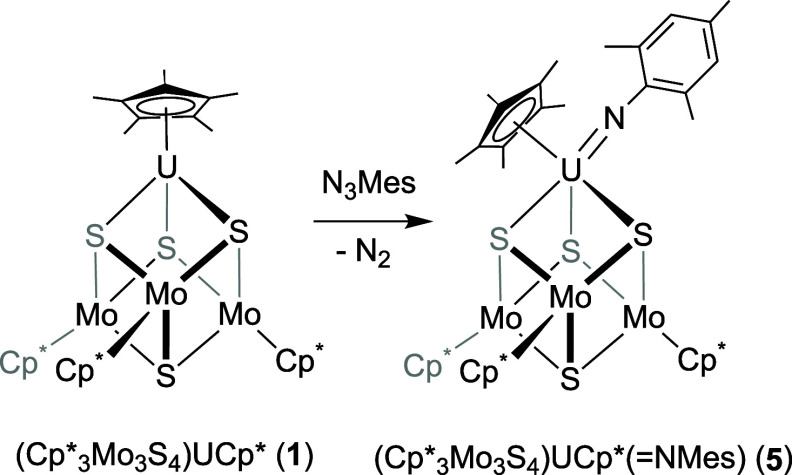
圖5.(Cp?Mo?S?)CpU (=NMes)(5)的合成。
總結與展望
該研究系統探究了氧化還原活性MoS?金屬配體表面低價鈾與水的反應性,明確鈾與金屬配體協同活化水的機制,成功分離穩定鈾氫氧化物中間體,通過多種途徑合成鈾-氧代類似物并借等電子模型分析其不穩定因素。后續研究將聚焦改良金屬配體提升鈾-氧代化合物穩定性,推動鈾化學及催化研究進程,為鈾基催化劑在能源、環境等領域應用奠定理論基礎,有望突破現有催化應用局限,開拓鈾基催化劑新應用場景。